喬治·丘奇實驗室再啟新篇章 獲拜耳投資,以非天然氨基酸與工程化大腸桿菌重塑蛋白質藥物研發未來
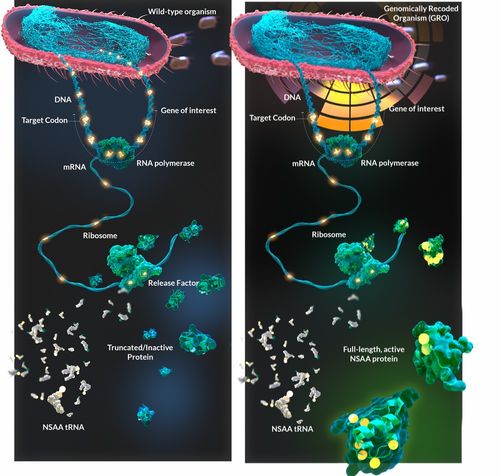
在合成生物學與生物醫藥的交叉前沿,傳奇科學家喬治·丘奇(George Church)教授的實驗室再次成為焦點。其最新孵化的公司成功獲得了醫藥巨頭拜耳(Bayer)的顯著投資,旨在通過一項融合了前沿理論與工程智慧的顛覆性策略——利用非天然氨基酸優化蛋白質藥物研發,并改造大腸桿菌打造更高效的“細胞工廠”,為下一代生物療法與網絡技術開發開辟全新路徑。
核心突破:非天然氨基酸的精準引入
傳統蛋白質藥物,如抗體、酶替代療法等,雖然療效顯著,但其功能與穩定性往往受限于自然界存在的20種標準氨基酸。喬治·丘奇實驗室所推動的技術核心,在于突破這一天然限制。通過擴展生物的遺傳密碼,將非天然氨基酸(unnatural amino acids, UAAs)精準、特異性地整合到目標蛋白質的特定位置。這些UAAs攜帶著自然界不存在的化學基團,如特殊的反應活性手柄、熒光標記、或能增強穩定性的特殊結構。這使得研究人員能夠:
- 賦予蛋白質全新功能:例如,為抗體藥物連接上更高效、更可控的細胞毒素,實現更精準的靶向治療,或引入可進行“點擊化學”反應的基團,便于后續的定點修飾與偶聯。
- 增強藥物穩定性與半衰期:通過引入能形成特殊交聯或具有更強疏水性的氨基酸,提高蛋白質在體內的穩定性,減少給藥頻率。
- 創建全新的藥物作用機制:為蛋白質引入全新的催化活性或調節功能,開發出針對“不可成藥”靶點的新型療法。
工程基石:改造大腸桿菌作為高效“智能工廠”
要實現非天然氨基酸的大規模、低成本整合,必須有一個強大且可控的生產平臺。研究團隊將目光投向了生物學中最經典的模式微生物——大腸桿菌。通過對大腸桿菌進行深度工程化改造,他們旨在將其打造為生產這些“增強型”蛋白質藥物的超級工廠:
- 重構蛋白質合成機器:改造核糖體、tRNA、氨酰-tRNA合成酶等核心組件,使其能準確識別并利用非天然氨基酸,確保翻譯的保真度與效率。
- 優化代謝與供給途徑:設計大腸桿菌的代謝網絡,使其能高效合成或攝取非天然氨基酸前體,確保生產原料的充足供應。
- 強化生產與折疊能力:工程化細菌的分泌系統和分子伴侶網絡,提高復雜蛋白質的正確折疊率和產量,滿足工業化生產需求。大腸桿菌生長快速、培養成本低廉、遺傳工具成熟,一旦改造成功,將能極大降低新型蛋白質藥物的開發與生產成本。
戰略協同:拜耳投資與網絡技術開發的遠景
拜耳作為全球領先的生命科學企業,此次投資不僅是對該技術平臺科學潛力的認可,更是其布局下一代生物制藥技術的關鍵一步。雙方的合作有望加速將該平臺應用于腫瘤學、心血管疾病、罕見病等領域的創新藥物研發。
值得注意的是,該公司的愿景并未止步于藥物研發。其技術中涉及的“遺傳密碼重編程”與“細胞工廠的精細化調控”,與網絡技術開發(此處指生物分子網絡、合成基因回路的設計與控制)深度關聯。通過將細胞視為一個可編程的生化反應網絡,利用工程學原理設計和構建基因控制回路,可以實現藥物生產的動態調節、按需釋放,甚至在未來開發出能感知體內疾病信號并自動生產治療性蛋白質的“智能活體療法”。這標志著從靜態生產到動態智能系統的跨越,為治療學帶來了前所未有的可能性。
****
喬治·丘奇實驗室的此次成果,是合成生物學“設計-構建-測試-學習”循環的又一次卓越體現。通過將非天然氨基酸化學、遺傳密碼擴展技術與微生物代謝工程、網絡控制理論深度融合,他們正試圖重新定義蛋白質藥物的邊界。在拜耳等產業巨頭的加持下,這項技術有望從實驗室快速走向臨床應用,不僅可能催生出一系列療效更優、機制更新的“超級藥物”,更可能從根本上改變生物藥物的研發和生產范式,推動醫療健康產業進入一個更加精準、高效和智能的新時代。
如若轉載,請注明出處:http://www.cnbaidianfeng.com/product/47.html
更新時間:2026-02-22 18:40:36